|
Доклад: Расчет коэффициентов активности. Личный опытДоклад: Расчет коэффициентов активности. Личный опытНе так давно я вплотную столкнулся с расчетами коэффициента активности растворов электролитов. Нельзя сказать, что раньше я никогда не производил таких расчетов, однако сейчас у меня возникли некоторые вопросы, связанные с расчетами в области высоких концентраций. Известно, что до ионной силы 0,01М коэффициент активности (f) хорошо описывается расширенной формулой Дебая-Хюккеля:
где z - заряд иона; I - ионная сила раствора; P - параметр Килланда, зависящий от размера иона; A = 0,509 при 250С ; B = 0,328 при 250С . Ионная сила раствора равна
где Ci - концентрация ионов одного вида в исследуемом растворе. Для области большей ионной силы, самой распространенной является следующая формула:
Эта формула предполагает увеличение коэффициента активности после некоего значения ионной силы. Большинство исследователей предпочитают в своих работах не упоминать об условиях, при которых следует от формулы (1) переходить к формуле (3). В связи с этим я предпринял собственные исследования, благо в моем распоряжении была программа IonCalc ( Программу можно получить здесь.). Поскольку я располагал справочными данными ("Краткий химический справочник" В.А.Рабиновича и З.Я.Хавина, изд. "Химия",1977г.) об экспериментально полученных значениях коэффициента активности, то работа состояла в сопоставлении этих данных с расчет ными. Расчеты я производил по формуле (1), так как применение формулы (3) только усугубляло расхождение между экспериментальными и расчетными данными. В справочнике приведены экспериментально полученные данные о среднем коэффициенте активности растворов солей. Средний коэффициент активности составляют коэффициенты активности аниона и катиона следующим образом: f срm+n = fMm + fAn , где
fM и fA - коэффициенты активности катиона и аниона: m и n - стехиометрические коэффициенты исследуемой соли MmAn. Если распоряжаться этой формулой, то можно легко рассчитать средний коэффициент активности и сравнить его с экспериментальным. Проведенные мной расчеты представлены в таблице, которая содержит сведения об относительной разнице в процентах между экспериментальными и расчетными данными. Относительная погрешность представлена в двух видах: среднеарифметическая величина погрешности (первое число) и максимальная погрешность в серии расчетов (второе число). Таблица 1.*)
1) AgNO3 , HCl, HNO3 , KBr, KCl, KOH, NaCl, NaOH, NH4Cl, NaCH3COO, NaNO3 , KNO3 . 2) BaCl2 , CaCl2 , FeCl2 , MgBr2 , MgCl2 , Ca(NO3)2 , Co(NO3)2 , Cu(NO3)2. 3) K2CrO4, K2SO4, Na2CrO4, (NH4)2SO4, Na2SO4, Na2CO3, K2CO3 . 4) ZnSO4, MgSO4, MnSO4, Cu SO4 . Расчеты показывают, что для ионной силы в 0,3М максимальная погрешность составляет 5-6%. Необъясненным остается тот факт, что коэффициент активности сульфатов двухзарядных металлов очень высок в сравнении с экспериментальными данными. Также высок средний коэффициент активности серной кислоты. Он составляет 0,266 для раствора с ионной силой 0,3 М, в то время как расчеты предоставляют величину 0,517. |
|
|
| 17.06.2012 |
| Большое обновление Большой Научной Библиотеки |
| 12.06.2012 |
| Конкурс в самом разгаре не пропустите Новости |
| 08.06.2012 |
| Мы проводим опрос, а также небольшой конкурс |
| 05.06.2012 |
| Сена дизайна и структуры сайта научной библиотеки |
| 04.06.2012 |
| Переезд на новый хостинг |
| 30.05.2012 |
| Работа над улучшением структуры сайта научной библиотеки |
| 27.05.2012 |
| Работа над новым дизайном сайта библиотеки |


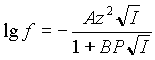
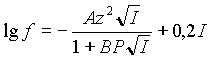 .
.