|
Реферат: Арилгалогениды и фенолыРеферат: Арилгалогениды и фенолыФенолы Фенолами называют соединения общей формулы Ar-OH, Они отличаются от спиртов тем, что в них гидроксильная группа непосредственно присоединена к ароматическому кольцу. В зависимости от количества гидроксильных групп фенолы различаются по атомности: одноатомные, двухатомные, трехатомные и т.д., для бензола до шестиатомных. Для метилфенолов принято специальное название - крезолы.
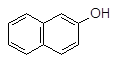
Фенол 4-Метилфенол (п-крезол) a-Нафтол b-Нафтол Производные фенолов широко распространены в природе. Тимол является антисептиком и используется в парфюмерии. Эвгенол содержится в различных эфирных маслах, в том числе в гвоздичном масле.
2-Изопропил-5-метилфенол 4-Аллил-2-метоксифенол (тимол) (эвгенол) Ароматическое ядро, непосредственно связанное с гидроксильной группой оказывает сильное влияние на ее поведение. Это влияние так велико, что фенолы и спирты представляют собой разные классы органических соединений. Они отличаются, прежде всего, по кислотности. Значения рКа большинства спиртов составляет около 18, в то время как фенолов - менее 11. Сравним, например, циклогексанол и фенол:
Циклогексанол Фенол рКа = 18 рКа = 9.9 Фенолы являются более сильными кислотами, чем вода, в то время как спирты более слабыми, чем вода. В отличие от спиртов фенолы со щелочью дают соли – феноксиды (феноляты), не разрушающиеся водой, но разлагающиеся более сильной угольной кислотой.
Приведенные реакции используются для разделения фенолов, спиртов и карбоновых кислот. Фенолы, содержащие электроноакцепторные группы в ядре, имеют большую кислотность, чем сам фенол. Большая кислотность фенолов по сравнению со спиртами может быть объяснена тем, что электронная плотность в них с атома кислорода смещена на бензольное кольцо. Упр.10. Что происходит при пропускании диоксида углерода через водный раствор фенолята натрия? Напишите уравнение этой реакции. Арилгалогениды Соединения, в которых атомы галогенов присоединены к бензольному кольцу называют арилгалогенидами. Галогены в арилгалогенидах более устойчивы к нуклеофильному замещению, чем в алкилгалогенидах. Например, в 2-(3-хлорфенил)-1-хлорэтане при обычной температуре гидролизуется только тот атом хлора, который связан с насыщенным атомом углерода.
2-(3-Хлорфенил)-1-хлорэтан 2-(3-Хлорфенил)-1-этанол (1) Арилгалогениды не реагируют по механизму SN1, т.к. арил-катионы крайне неустойчивы и не могут образовываться. Они не могут реагировать и по механиз-му SN2, т.к. бензольное кольцо препятствует тыловой атаке по механизму SN2:
Хлорбензол можно нагревать со щелочью в течение нескольких дней без заметного прохождения реакций замещения:
Хлорбензол Арилгалогениды, в отличие от алкилгалогенидов, не дают положительной реакции при действии на них нитрата серебра в спирте. Свободные пары электронов на галогенах в них взаимодействуют с p-системой связей бензольного кольца. Мезомерный эффект (+М-эффект) галогенов не велик, т.к. активность их р-электронов мала. Индуктивный же эффект (-I-эффект, т.е. оттяжка электронной пары связи к галогену) всегда велик, и он наводит положительный заряд на связанный с ним атом углерода и далее на о- и п-атомы углерода бензольного кольца. Повышенная прочность галогенуглеродной связи в арилгалогенидах обусловлена двумя факторами: (1) aтом углерода в них sp2 гибридизован, и поэтому электроны на его орбиталях ближе к ядру, чем у sp3 гибридизованного углерода; (2) электронная пара на атомах галогена сопряжена с бензольным кольцом, и поэтому она частично двойная:
1.1. Нуклеофильное замещение по механизму отщепление- присоединение (ариновый механизм) Несмотря на малую реакционную способность арилгалогенидов они довольно широко используются в промышленности для получения различных ароматических соединений. Наиболее легко нуклеофильному замещению подвергается йод. В жестких условиях арилгалогениды (за исключением фторидов) вступают в реакции замещения.
Феноксид натрия При замещении хлора в пара-хлортолуоле на гидроксильную группу в аналогичных условиях образуется смесь пара- и мета-крезолов.
п-Хлортолуол п-Крезол м-Крезол При действии амида калия на о-хлоранизол в жидком аммиаке образуется м-аминоанизол .
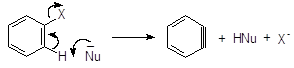
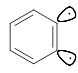
о-Хлоранизол м-Аминоанизол Такой результат можно объяснить с помощью механизма отщепления- присоеди-нения SNAr. На первой стадии нуклеофил действует как основание, отщепляя протон в орто-положении к атому галогена ароматического субстрата. Отщепляется именно орто-протон, самый «кислый» (кислотность убывает в ряду орто-Н > мета-Н > параН >). На второй стадии быстро отщепляется галоген и образуется дегидробензол.
Дегидробензол или бензин Далее следует стадия присоединения HNu к молекуле дегидробензола:
Дегидробензол очень легко вступает в реакции присоединения с любыми нуклеофилами, например, с растворителем. Атака будет происходить по обоим троесвязанным атомам углерода, что и приводит к образованию смеси продуктов как в случае п-хлортолуола. В о-хлоранизоле атака происходит по одному атому из-за стерических препятствий. Следует иметь в виду, что орбитали, образующие третью связь в молекуле дегидробензола, не перекрываются с р-орбиталями бензольного кольца и, следовательно, не участвуют в сопряжении. Они находятся в той же плоскости, что и кольцо. Между собой они перекрываются слабо, поэтому третья связь и очень реакционноспособна.
Упр.1. Напишите реакцию п-хлортолуола с амидом натрия и опишите ее механизм. Упр.2. Напишите реакции хлорбензола при повышенной температуре в присутствии меди с (а) цианидом натрия и (б) с ацетатом натрия. Ответ. (а) Бензонитрил При использовании медного катализатора эти реакции проходят легче (Ульман). Упр.3. При замещении хлора в орто-хлортолуоле на гидроксильную группу при нагревании с 15%-м водным раствором щелочи под давлением образуется смесь двух крезолов. Напишите эту реакцию и опишите е механизм. 1.2. Нуклеофильное замещение по механизму присоединение- отщепление Этот механизм, обозначаемый SNAr, характерен для арилгалогенидов, содержащих активирующие элетроноакцепторные заместители в орто- и пара-положениях кольца.
о-нитрохлорбензол о-нитрофенол
2,4-динитро-N,N-диметиланилин При наличии электроноакцепторных групп в мета-положении аналогичного активирующего эффекта не наблюдается. Например, м-нитрохлорбензол в аналогичную реакцию не вступает. Описанные реакции проходят по механизму присоединения-отщепления. Реакция осуществляется в две стадии, из которых лимитирующей обычно является первая. В качестве промежуточного соединения образуется s-комплекс (комплекс Мейзенгеймера), распадающийся далее на продукты реакции. В некоторых случаях комплексы Мейзенгеймера могут быть выделены.
s-Комплекс Незамещенный хлорбензол в этих условиях совершенно инертен. Интересно отметить, что фтор в динитрофторбензоле замещается еще легче, чем хлор. Поэтому 2,4-динитрофторбезол широко используется для введения 2,4-динитро-фенильного остатка, например, в концевые аминогруппы белков.
2,4-Динитрофторбензол Напомним, что в предельных соединениях хлор подвижнее фтора. Это объясняется тем, что хотя фтор и подает связанному с ним атому углерода свободные электроны, но в гораздо меньшей степени, чем хлор. Упр.4. Опишите механизм реакции:
Ответ:
Упр.5. Напишите реакции и опишите механизм: (а) 2,4,6-тринитрохлорбен-зола с водным раствором бикарбоната натрия с последующим подкислением; (б) р-нитробензола с метоксидом натрия в метаноле при 100оС: (в) о-нитробензо-ла с этиламином в этаноле при 160оС. Упр.6. Напишите реакции 2,4-динитрохлорбензола: (а) с анилином в этаноле при 95оС, (б) с гидразином в этаноле при нагревании, (в) с аммиаком в воде при 170оС под давлением. |
|
|
| 17.06.2012 |
| Большое обновление Большой Научной Библиотеки |
| 12.06.2012 |
| Конкурс в самом разгаре не пропустите Новости |
| 08.06.2012 |
| Мы проводим опрос, а также небольшой конкурс |
| 05.06.2012 |
| Сена дизайна и структуры сайта научной библиотеки |
| 04.06.2012 |
| Переезд на новый хостинг |
| 30.05.2012 |
| Работа над улучшением структуры сайта научной библиотеки |
| 27.05.2012 |
| Работа над новым дизайном сайта библиотеки |


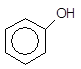

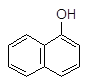
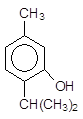
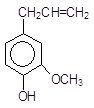

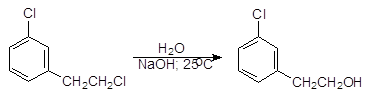
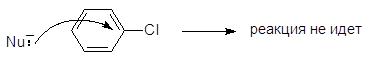
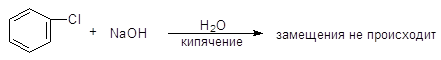
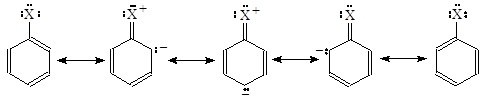
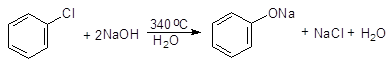 (2)
(2)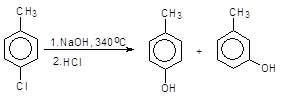 (3)
(3)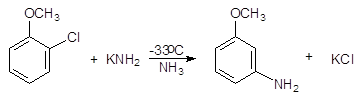 (4)
(4)
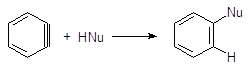
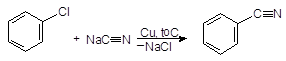
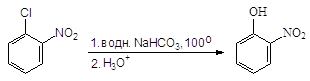 (5)
(5)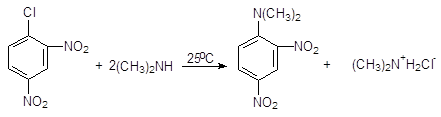 (6)
(6)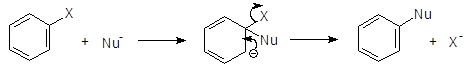 (М 1)
(М 1)